基因治療的概念是在20世紀(jì)70年代初提出來(lái)的����,最初的概念是引入一個(gè)正常的基因來(lái)取代一個(gè)突變基因,雖然現(xiàn)在有更多的替代方法�����,如基因編輯和堿基編輯�����,但它仍然是我們高度依賴的主要策略之一���。
2012年歐洲批準(zhǔn)Glybera��,這是西方國(guó)家首個(gè)基因治療產(chǎn)品����,也是全球首個(gè)針對(duì)基因疾病的基因治療�。盡管Glylbera在商業(yè)上并不成功,但它打開了基因治療的大門。在隨后的幾年里�,一些基因治療產(chǎn)品陸續(xù)涌入市場(chǎng),Strimvelis于2016年在歐洲獲得批準(zhǔn)���,CAR-T療法(Kymriah和Yescarta)和Luxturna分別于2017年獲得美國(guó)食品和藥物管理局(FDA)的批準(zhǔn)�����。
據(jù)弗若斯特沙利文數(shù)據(jù)顯示���,2015年以來(lái),全球基因治療行業(yè)開始高速發(fā)展�����。到2016年���,全球和國(guó)內(nèi)基因治療市場(chǎng)規(guī)模分別為5,040萬(wàn)美元、1,500萬(wàn)元�����;2020年全球基因市場(chǎng)規(guī)模有所增長(zhǎng)����,達(dá)到20.8億美元��。據(jù)預(yù)計(jì)����,2025年��,全球市場(chǎng)和國(guó)內(nèi)市場(chǎng)將分別達(dá)到近305.4億美元和178.9億元�����?��;蛑委煶蔀槔^小分子藥物�����、抗體藥物之后的生物醫(yī)藥的第三次產(chǎn)業(yè)革命��。
基因治療的發(fā)展階段
基因治療從發(fā)明到初步應(yīng)用以及目前的蓬勃發(fā)展���,經(jīng)歷了下面的四個(gè)階段:

基礎(chǔ)研究階段(1909-1973)
最早,Wilhelm Johannsen創(chuàng)造了“基因”一詞����,然后在大約半個(gè)世紀(jì)后�����,F(xiàn)rancis Crick和James Watson發(fā)現(xiàn)了DNA的雙螺旋結(jié)構(gòu)��。細(xì)菌中基因轉(zhuǎn)移的基本原理在20世紀(jì)60年代被發(fā)現(xiàn)���,隨后被發(fā)展為真核生物轉(zhuǎn)染技術(shù)。到20世紀(jì)70年代����,限制酶和連接酶的應(yīng)用構(gòu)成了基因操縱的基礎(chǔ),重組DNA技術(shù)使研究人員能夠?qū)⑦x定的治療基因引入工程載體���。隨著發(fā)現(xiàn)病毒轉(zhuǎn)移遺傳物質(zhì)的能力���,病毒載體已成為一種有前途的有效基因轉(zhuǎn)移工具�����。這些技術(shù)進(jìn)步使科學(xué)家能夠創(chuàng)建將特定遺傳物質(zhì)轉(zhuǎn)移到靶細(xì)胞中的基因治療載體�����。
早期的基因治療臨床實(shí)踐(1989–2003)
基因治療的第一次臨床實(shí)踐開始于1989年,一種逆轉(zhuǎn)錄病毒被用于在腫瘤浸潤(rùn)淋巴細(xì)胞上表達(dá)新霉素抗性標(biāo)記物��,該標(biāo)記物用于黑色素瘤免疫治療中追蹤浸潤(rùn)淋巴細(xì)胞�����。1990年�����,賓夕法尼亞大學(xué)的科學(xué)家對(duì)一名四歲的女孩Ashanti Desilva進(jìn)行了第一次成功的基因治療臨床試驗(yàn)���。她被診斷為嚴(yán)重聯(lián)合免疫缺陷(SCID)����,研究人員使用逆轉(zhuǎn)錄病毒載體將腺苷脫氨酶(ADA)的正??截愞D(zhuǎn)移到她的T細(xì)胞。目前她已經(jīng)可以正常生活����。
然而,病毒載體的使用伴隨著一些不良事件���,如插入突變和免疫反應(yīng)����,這阻礙了臨床基因治療的進(jìn)展。2000年�,巴黎的歐洲研究人員報(bào)告了一項(xiàng)X連鎖SCID基因治療的成功臨床試驗(yàn)。然而��,20名接受治療的兒童中有5名在后期發(fā)展為白血病����,這是因?yàn)樵谳d體引入轉(zhuǎn)基因后激活了一種癌基因。與此同時(shí)���,1999年����,Jesse Gelsinger��,一名18歲的男孩���,被診斷患有一種罕見的代謝性疾病,他自愿成為接受編碼鳥氨酸轉(zhuǎn)氨酶基因治療的患者����。然而不幸的是��,其因大規(guī)模凝血障礙和隨后的多器官衰竭而死亡��,成為基因治療的第一位死亡患者����。盡管這些挫折減緩了基因治療的進(jìn)展��,但它們也展示了基因治療的潛力及其光明的未來(lái)�。
繁榮發(fā)展階段(2003-2022)
2003年,中國(guó)國(guó)家食品藥品監(jiān)督管理局(SFDA)批準(zhǔn)了Gendicine����,這是首款用于頭頸部癌癥的基因治療產(chǎn)品。兩年后�,SFDA批準(zhǔn)了Oncorine,這是第一種用于鼻咽癌的溶瘤病毒����。十年后的2012年,歐洲藥品管理局(EMA)批準(zhǔn)了首個(gè)針對(duì)脂蛋白脂酶缺乏癥的基因治療產(chǎn)品Glybera�����,臨床試驗(yàn)數(shù)量幾乎翻了一番。
首個(gè)體外基因治療產(chǎn)品Strimvelis于2016年獲得EMA批準(zhǔn)���。2017年�,F(xiàn)DA批準(zhǔn)了兩種嵌合抗原受體(CAR)T細(xì)胞產(chǎn)品Kymriah和Yescarta����,這是為未來(lái)產(chǎn)品鋪平道路的關(guān)鍵里程碑。Luxturna是FDA批準(zhǔn)的首個(gè)用于Leber先天性黑蒙(LCA)的體內(nèi)AAV基因治療產(chǎn)品����,并于2017年獲得批準(zhǔn)。2019年����,F(xiàn)DA批準(zhǔn)了迄今為止最昂貴的藥物Zolgensma,這是一種AAV產(chǎn)品��,適用于兒童脊髓性肌肉萎縮癥��。批準(zhǔn)的基因治療產(chǎn)品數(shù)量每年都在增加���。
未來(lái)的發(fā)展(2022–2025)
根據(jù)之前的臨床試驗(yàn)和目前批準(zhǔn)的產(chǎn)品��,這一前景廣闊的醫(yī)學(xué)領(lǐng)域似乎比以往任何時(shí)候都發(fā)展得更快�,預(yù)計(jì)在不久的將來(lái)會(huì)有數(shù)十種新的產(chǎn)品獲批。我們正在逐步將基因治療納入更廣泛的疾病治療領(lǐng)域�����。
癌癥基因治療的臨床概況
目前基因治療的臨床應(yīng)用可分為三個(gè)主要領(lǐng)域:癌癥����、遺傳性疾病和傳染病���。
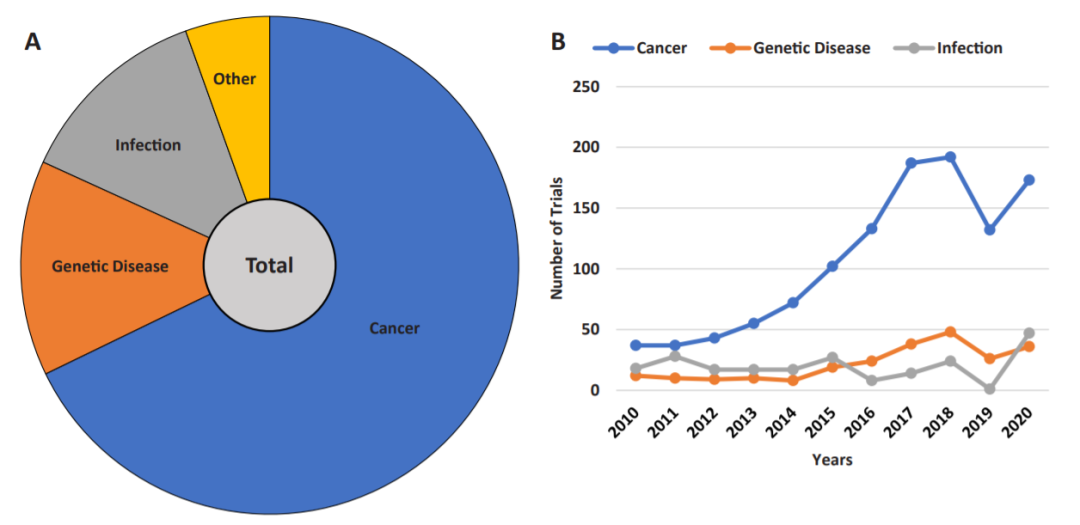
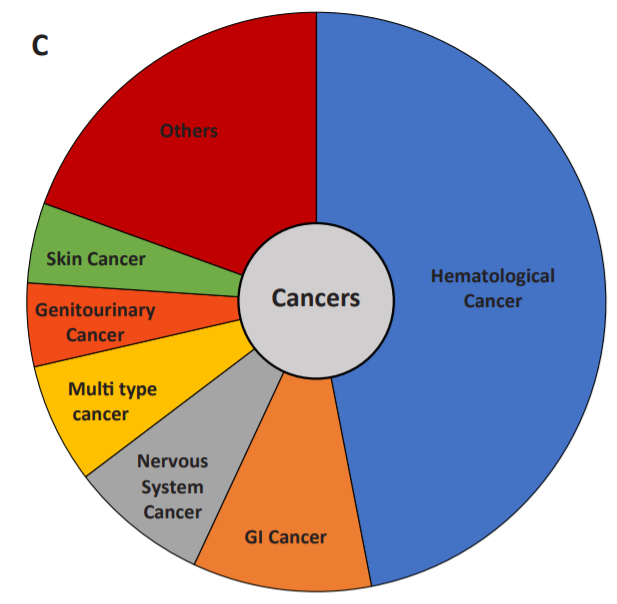
雖然基因治療被認(rèn)為是對(duì)某些遺傳疾病的治療����,但癌癥是基因治療最常見的疾病�。從2010年到2020年,癌癥相關(guān)臨床試驗(yàn)占所有研究的大多數(shù)���。血液學(xué)癌癥是研究最多的癌癥�,其次是胃腸道和神經(jīng)系統(tǒng)癌癥��。
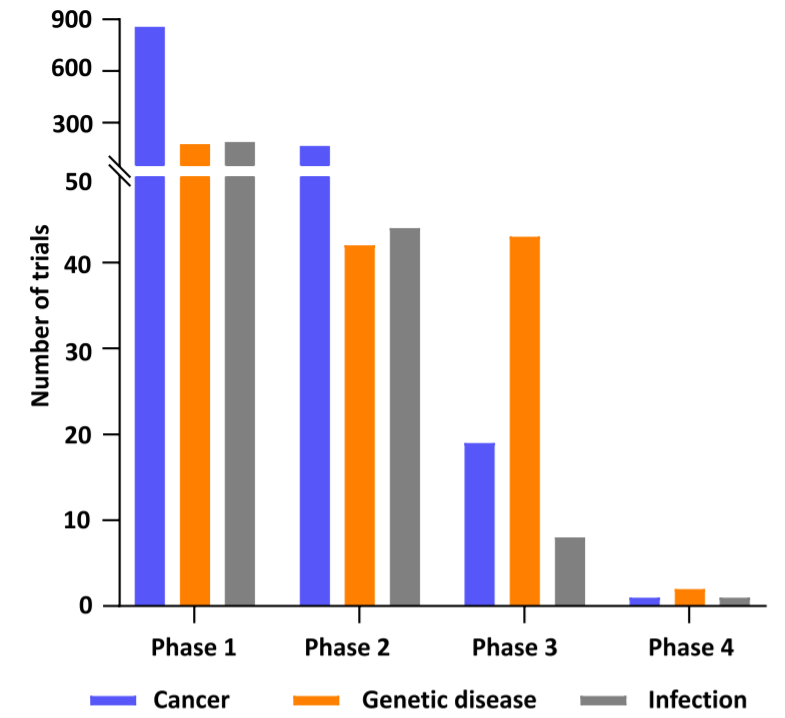
CAR-T細(xì)胞是免疫治療中最知名和最成功的基因治療應(yīng)用之一���。從目前針對(duì)癌癥的臨床試驗(yàn)來(lái)看���,大多數(shù)試驗(yàn)都處于第一階段�。第2階段臨床試驗(yàn)的數(shù)量也很高�,但只有少數(shù)進(jìn)行了隨后的第3階段試驗(yàn)。
迄今為止�,已批準(zhǔn)幾種基因治療產(chǎn)品用于治療癌癥,包括gendicine���、oncorine�、rexin-G��、imlygic�、delytact和八種CAR-T細(xì)胞,包括kymriah����、yescarta、tecartus�����、breyanzi�����、abecma、ARI-0001����、carteyva和carvykti。
遺傳疾病基因治療的臨床概況
與癌癥不同�����,大多數(shù)這類疾病��,如地中海貧血�����、Deschene肌營(yíng)養(yǎng)不良(DMD)和囊性纖維化�����,都是遺傳性的���。半數(shù)以上的臨床試驗(yàn)集中于代謝障礙、眼部疾病和凝血障礙�。進(jìn)一步,臨床試驗(yàn)最多的遺傳疾病是SMA、DMD���、血友病B��、ADA-SCID和β-地中海貧血��。
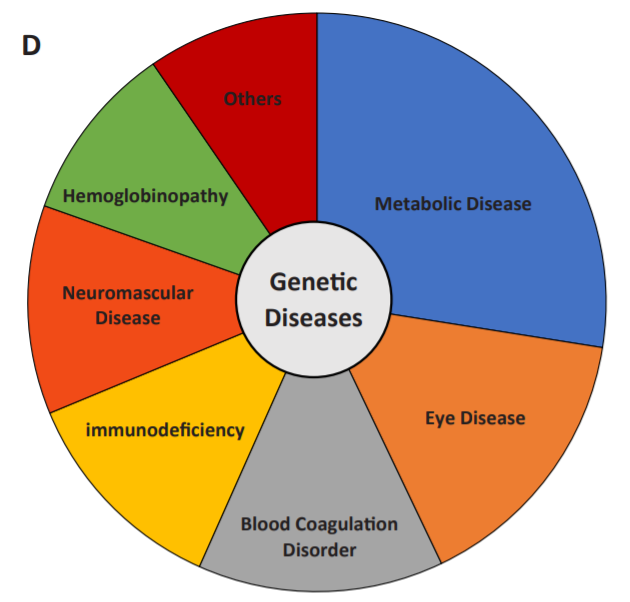
與癌癥相比��,遺傳性疾病的3期臨床試驗(yàn)比例更高�����。LCA�����、SMA�����、ATTR淀粉樣變��、原發(fā)性高草酸尿癥�、淀粉樣神經(jīng)疾病�、DMD、脂蛋白脂酶缺乏癥、家族性乳糜微粒血癥綜合征和高甘油三酯血癥是3期試驗(yàn)中正在研究的遺傳性疾病��。此外����,還有兩項(xiàng)4期臨床試驗(yàn),包括兩種FDA和EMA批準(zhǔn)的基因治療產(chǎn)品��,Spinraza和Zolgensma治療SMA�����。
盡管遺傳性疾病臨床試驗(yàn)的總數(shù)少于癌癥��,但目前批準(zhǔn)用于遺傳性疾病的產(chǎn)品數(shù)量更高(20對(duì)13)���。迄今為止,已批準(zhǔn)ADA-SCID��、DMD��、SMA����、LCA、B型地中海貧血和多種代謝疾病的產(chǎn)品。
傳染病及其他基因治療的臨床概況
人們一直在努力尋找治療一些最嚴(yán)重傳染病的方法����,如AIDS或瘧疾,基因治療也不例外�。盡管它們只占基因治療臨床試驗(yàn)的一小部分,但隨著新冠肺炎大流行的出現(xiàn)����,自2019年12月以來(lái)啟動(dòng)了29項(xiàng)針對(duì)新冠肺炎的試驗(yàn)。艾滋病��、新冠肺炎�、瘧疾、埃博拉��、丙型肝炎��、人乳頭瘤病毒感染和乙型肝炎是臨床試驗(yàn)次數(shù)最多的傳染病��。
大多數(shù)臨床試驗(yàn)使用疫苗接種策略來(lái)誘導(dǎo)對(duì)相應(yīng)疾病的免疫力�����。只有少數(shù)處于晚期階段的基因療法�����,即使用DNA作為乙肝病毒載體的基因療法。從獲批的產(chǎn)品來(lái)看�����,基因治療策略在有效解決傳染病方面還有很長(zhǎng)的路要走����。
此外,除了癌癥�����、遺傳病和傳染病外�,基因治療的研究也已用于外周血管疾病����、骨關(guān)節(jié)炎、糖尿病視網(wǎng)膜病變���、黃斑變性���、冠狀動(dòng)脈疾病��、心肌缺血和梗死�����、糖尿病神經(jīng)病變�����、過敏性鼻炎�、心力衰竭和增生性瘢痕�����。
基因治療臨床實(shí)驗(yàn)的地區(qū)分布
20世紀(jì)90年代初���,美國(guó)國(guó)家衛(wèi)生研究所進(jìn)行了第一次成功的基因治療臨床試驗(yàn)���。盡管自那時(shí)以來(lái),美國(guó)的基因治療臨床試驗(yàn)比任何其他國(guó)家都多���,但中國(guó)率先批準(zhǔn)了首個(gè)可商業(yè)化的基因治療產(chǎn)品(Gendicine)����。20世紀(jì)90年代末,歐洲的幾個(gè)國(guó)家是最早實(shí)施基因治療的國(guó)家之一���。
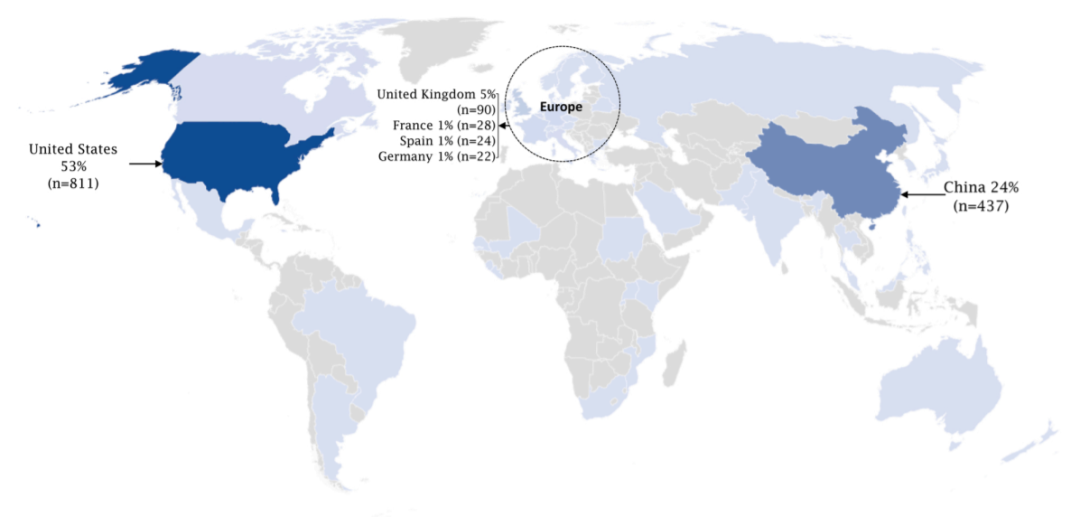
目前�����,美國(guó)和中國(guó)主導(dǎo)了基因治療臨床試驗(yàn)�,約占所有試驗(yàn)的80%�。近年來(lái),包括英國(guó)���、法國(guó)��、西班牙和德國(guó)在內(nèi)的其他幾個(gè)國(guó)家在這一前景廣闊的領(lǐng)域表現(xiàn)出色����。在多個(gè)國(guó)家的研究所或大學(xué)的合作下�,正在進(jìn)行的臨床試驗(yàn)越來(lái)越多�。2010年至2020年,基因治療臨床試驗(yàn)的數(shù)量翻了一番����。
小結(jié)
基因治療從進(jìn)入臨床實(shí)踐至今已有約三十年�����?����?v觀上個(gè)世紀(jì)基因治療的發(fā)展趨勢(shì)�,我們已經(jīng)進(jìn)入了一個(gè)新時(shí)代�����,過去十年獲批的基因治療產(chǎn)品數(shù)量不斷增加就是證明��。并且隨著遺傳學(xué)及生物技術(shù)的發(fā)展突破��,如CRISPR-CAS基因編輯��,使得基因療法可治療疾病的種類更為廣闊�����。
對(duì)基因治療臨床試驗(yàn)的十年趨勢(shì)分析表明��,雖然基因療法主要用于癌癥和遺傳性疾病�����,但包括艾滋病、瘧疾和人乳頭瘤病毒等多項(xiàng)傳染病臨床試驗(yàn)都已進(jìn)入臨床晚期研究階段����。在過去10年,體外基因治療已經(jīng)取得了一定的進(jìn)展�����,目前的管線眾多�����,而體內(nèi)基因治療也將會(huì)在未來(lái)十年迎來(lái)新的發(fā)展高潮���。
(來(lái)源:醫(yī)前沿)