(一)生物制品受理情況
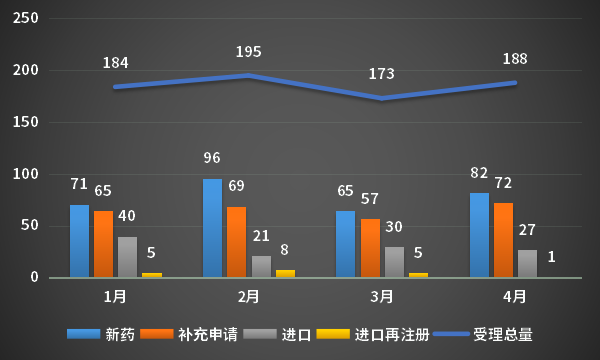
4月,CDE承辦新的生物制品注冊申請受理號共計188個�,新藥82個,補充申請72個��,進口27個���,進口再注冊1個���;2023年1-4月CDE生物制品各申請類型受理情況詳見圖8。
圖8 2023年1-4月CDE生物制品各申請類型受理情況
1.生物制品1類新藥申報情況
4月���,共76個生物制品1類新藥受理號獲得承辦����,其中��,臨床試驗申請71個��,上市申請5個�����,目前均已進入相應序列排隊待審;下表為4月新承辦的生物制品1類創(chuàng)新藥��。
表6 2023年4月新承辦的生物制品1類新藥

(二)生物制品完成審評情況
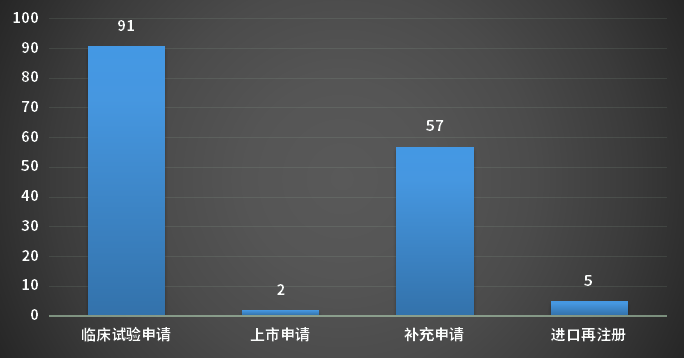
4月��,CDE完成審評的生物制品注冊申請165個(以受理號計)�,其中新藥申請受理號81個,進口受理號12個����,補充申請57個;以審評任務類別統(tǒng)計(以受理號計)��,臨床試驗申請91個��,上市申請2個���;2023年4月CDE生物制品各審評任務類別完成審評情況詳見圖9�;
圖9 2023年4月CDE生物制品各審評任務類別完成審評情況
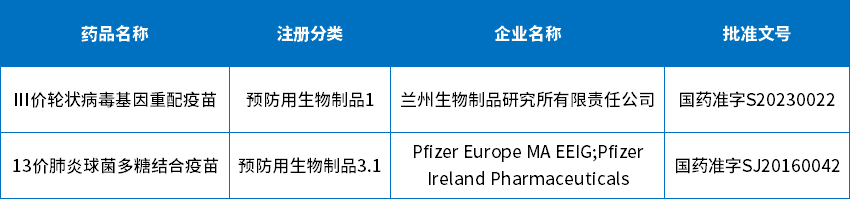
在受理號審評結(jié)論方面:批準臨床112個����,批準生產(chǎn)1個����,批準進口1個�����,批準再注冊5個���,未被批準6個;4月份有1個預防用生物制品1類新藥和1個3.1類預防用生物制品獲批上市���;下表為4月生物制品批準上市信息��。
表7 2023年4月生物制品獲批信息
(來源:藥智網(wǎng))