準(zhǔn)確把握全球未來生物醫(yī)藥產(chǎn)業(yè)布局方向
了解把握全球生物醫(yī)藥研發(fā)熱點技術(shù)對于我國科學(xué)布局生物醫(yī)藥關(guān)鍵技術(shù)研發(fā)方向���、制定更有針對性的創(chuàng)新扶持政策具有重要現(xiàn)實意義�?�?紤]到對已有專利等科研和產(chǎn)業(yè)化成果進(jìn)行分析的傳統(tǒng)研究范式無法突破“專利墻”制約����,為了更好地分析研判全球主要國家正在開展且尚未形成“專利墻”的生物醫(yī)藥技術(shù)科研布局方向�,我們創(chuàng)造性地從處于創(chuàng)新早期的全球科研項目立項入手,對目前全球主要國家的主要科研資助機(jī)構(gòu)近5年(2018年1月1日至2022年8月31日)所支持的27911個生物醫(yī)藥技術(shù)研究項目進(jìn)行大數(shù)據(jù)挖掘和分析��,綜合運(yùn)用無監(jiān)督短語抽取����、文本核心內(nèi)容篩選、短語挖掘和擴(kuò)充等AI技術(shù)并結(jié)合領(lǐng)域?qū)<因炞C�����,梳理出當(dāng)前全球主要國家生物醫(yī)藥技術(shù)前沿重點布局的30個熱點技術(shù)方向(見表1和圖1)���。這30個熱點技術(shù)既涵蓋基因編輯(Gene editing)���、藥物遞送(Drug delivery)����、誘導(dǎo)型人工多能干細(xì)胞(Induced pluripotent stem cell)等主流熱點���,也包含空間轉(zhuǎn)錄組學(xué)(Spatial transcriptomics)�����、異種移植(Xenotransplantation)�、相分離(Phase separation)等潛在研究熱點����,代表了發(fā)達(dá)國家未來生物醫(yī)藥產(chǎn)業(yè)的布局。
表1 全球生物醫(yī)藥技術(shù)研究關(guān)鍵技術(shù)點

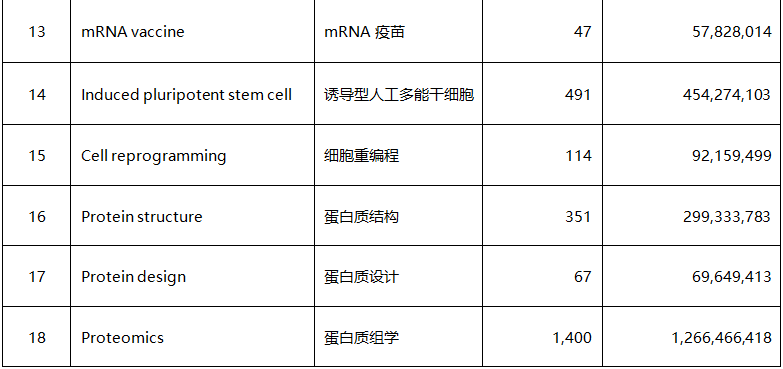
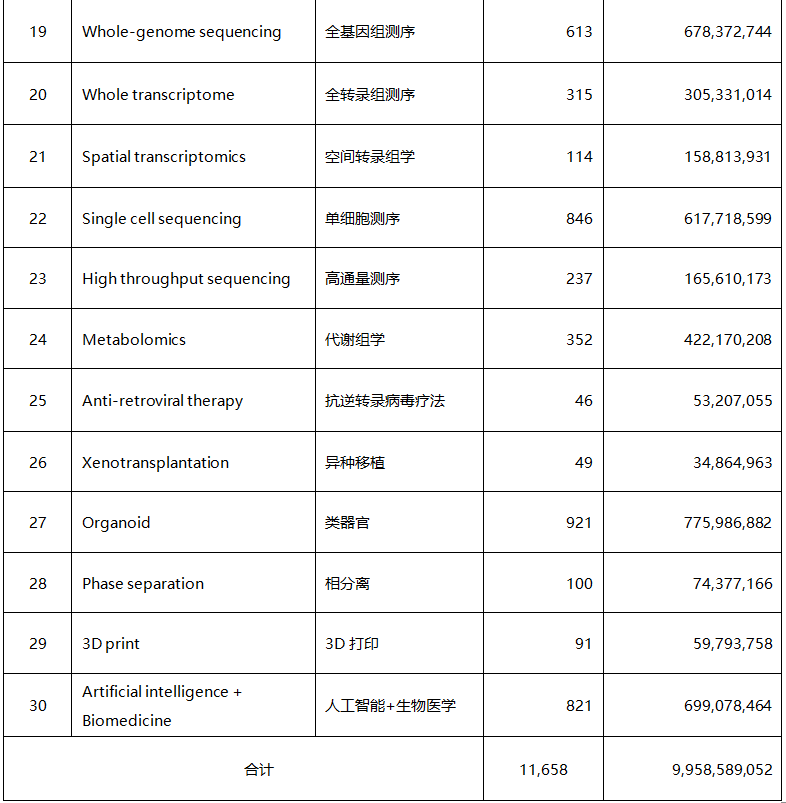
上述30個熱點技術(shù)領(lǐng)域覆蓋11658個在研科研項目�,占全部樣本的41.8%,共計得到99.59億美元的科研經(jīng)費(fèi)資助�����。其中�,關(guān)于基因編輯工具CRISPR-Cas技術(shù)的研究項目最多,達(dá)1478項����;關(guān)于蛋白質(zhì)組學(xué)技術(shù)的項目資助金額最多�,達(dá)12.66億美元�,占全部資助金額的12.7%。顯然����,這些關(guān)鍵技術(shù)點或是當(dāng)前生物醫(yī)藥的重點研究方向�����,或是涉及未來生物醫(yī)藥的關(guān)鍵共性技術(shù)��,或是未來生物醫(yī)藥創(chuàng)新技術(shù)相關(guān)的基礎(chǔ)原理研究����。可以預(yù)見����,這30個得到主要發(fā)達(dá)國家生物醫(yī)學(xué)科研機(jī)構(gòu)重點支持布局的技術(shù)領(lǐng)域?qū)⒃谖磥?年左右產(chǎn)生重大技術(shù)突破并在未來8—10年具備產(chǎn)業(yè)化條件�,從而創(chuàng)造出全球生物醫(yī)藥產(chǎn)業(yè)發(fā)展的新機(jī)遇。
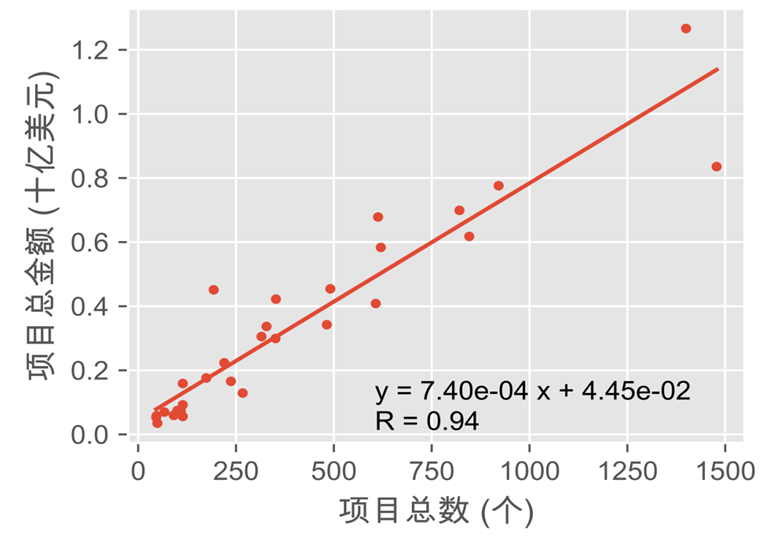
不同技術(shù)研究熱度不同。每類技術(shù)的項目數(shù)量與總資助金額高度正相關(guān)(見圖2)����,每類技術(shù)的研究項目數(shù)量和累計總資助金額基本可以反映該技術(shù)當(dāng)前研究熱度(見圖3)。其中��,CRISPR-Cas和蛋白質(zhì)組學(xué)無論是資助項目數(shù)量還是總資助金額�����,都遠(yuǎn)超其它技術(shù)點�����,在癌癥����、艾滋病等研究領(lǐng)域有著極為基礎(chǔ)性的應(yīng)用。例如����,天普大學(xué)2021年承接的,名為“CRISPR for Cure”的NIH資助研究項目(項目號:UM1AI164568)�����,致力于開發(fā)基于CRISPR的HIV治愈方法。斯克利普斯研究所(Scripps Research)連續(xù)5年(2018—2022年)承接名為“Chemical Proteomic Platforms for Radically Expanding Cancer Druggability”的NIH資助研究項目(項目號:R35CA231991)�����,致力于持續(xù)建設(shè)可用于研究癌癥成藥性的化學(xué)蛋白質(zhì)組學(xué)平臺�����。
圖1 關(guān)鍵技術(shù)點詞云圖(技術(shù)點單詞大小與資助總金額成正比)

圖2 關(guān)鍵技術(shù)點資助項目數(shù)量與總金額線性關(guān)系圖
不同技術(shù)資助強(qiáng)度不同�����。在全部30項關(guān)鍵技術(shù)中���,疫苗設(shè)計(233.75萬美元)、空間轉(zhuǎn)錄組學(xué)(139.31萬美元)�、mRNA疫苗(123.04萬美元)、代謝組學(xué)(119.94萬美元)��、抗逆轉(zhuǎn)錄病毒療法(115.67萬美元)的項目平均資助金額較高�����;CRISPR-Cas(56.54萬美元)�����、靶向蛋白質(zhì)降解(49.10萬美元)、免疫檢查點抑制劑(48.31萬美元)技術(shù)的項目平均資助金額相對偏低��。其中���,疫苗設(shè)計研究項目的平均資助金額達(dá)233.75萬美元���,是所有技術(shù)點中平均資助金額最高的,既表明新冠疫情背景下疫苗研究的重要性����,也說明疫苗研究耗資較大,需要較強(qiáng)的資金投入力度��。而技術(shù)點之間投入強(qiáng)度的差異性表明�����,不同技術(shù)點對于資金投入的需求存在客觀差異�,需要根據(jù)技術(shù)點本身的科研特性確定資助強(qiáng)度。
圖3 關(guān)鍵技術(shù)點研究熱度圖(圖形大小與資助總金額正相關(guān))
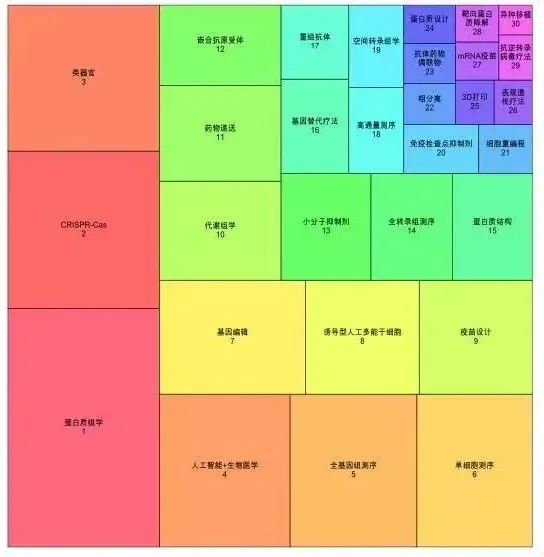
資助和承接主體呈現(xiàn)多樣化���。為了進(jìn)一步了解挖掘出來的30項關(guān)鍵技術(shù)的主要資助機(jī)構(gòu)和對應(yīng)的被資助研究單位分布情況��,有利于研究人員進(jìn)一步追蹤相關(guān)進(jìn)展�,課題組對重點資助機(jī)構(gòu)和被資助機(jī)構(gòu)排名前3的單位進(jìn)行了分析(詳見附件)。從資助方來看��,美國國立衛(wèi)生研究院(NIH)在大部分領(lǐng)域都是最大的資助方���,各出資機(jī)構(gòu)在基因編輯和藥物遞送等主流關(guān)鍵技術(shù)點上都有涉及�����,但在具體的關(guān)鍵技術(shù)點布局上存在差異���。例如,日本科學(xué)技術(shù)振興機(jī)構(gòu)(JST)在CRISPR-Cas��、免疫檢查點抑制劑(Immune checkpoint inhibitor)�����、類器官(Organoid)�、異種移植(Xenotransplantation)���、藥物遞送(Drug delivery)技術(shù)點上的資助項目領(lǐng)先于其它研究出資機(jī)構(gòu)���,德國科學(xué)基金會(DFG)則在表觀遺傳療法(Epigenetic therapy)�����、全轉(zhuǎn)錄組測序(Whole transcriptome)���、單細(xì)胞測序(Single-cell sequencing)、高通量測序(High-throughput sequencing)�����、代謝組學(xué)(Metabolomics)等技術(shù)點上的投入領(lǐng)先[1]�����。從被資助方來看��,高校是主要的項目承接方�����,斯坦福大學(xué)���、哈佛大學(xué)�、耶魯大學(xué)、杜克大學(xué)����、賓夕法尼亞大學(xué)、劍橋大學(xué)�����、約翰霍普金斯大學(xué)等傳統(tǒng)名校綜合研究能力較強(qiáng)����,在諸多技術(shù)點上都有較強(qiáng)的技術(shù)儲備。西奈山伊坎醫(yī)學(xué)院(Icahn School of Medicine at Mount Sinai)����、貝勒醫(yī)學(xué)院(Baylor College of Medicine)、麻省總醫(yī)院(Massachusetts General Hospital)��、波士頓兒童醫(yī)院(Boston Children’s Hospital)�、斯克利普斯研究所、索爾克生物研究所(Salk Institute for Biological Studies)等獨立醫(yī)學(xué)院�、醫(yī)院和非盈利研究機(jī)構(gòu)在個別技術(shù)點上承接研究項目較多�����,布局較為深入。
科學(xué)謀劃我國未來生物醫(yī)藥產(chǎn)業(yè)重點方向
在上文中���,我們梳理挖掘出了全球主要國家重點資助的30個關(guān)鍵生物醫(yī)藥技術(shù)�?��?梢灶A(yù)判�,這些重點投入的在研的關(guān)鍵技術(shù)中將會產(chǎn)生重大技術(shù)突破�,從而創(chuàng)造未來生物醫(yī)藥產(chǎn)業(yè)的眾多發(fā)展機(jī)遇。當(dāng)前�,我國正在迎來生物醫(yī)藥產(chǎn)業(yè)的黃金發(fā)展期,生物醫(yī)藥創(chuàng)新能力已從全球第三梯隊進(jìn)入到第二梯隊�����。在這一階段�,我們不但要密切跟蹤全球生物醫(yī)藥關(guān)鍵技術(shù)走勢,更要基于我國科研基礎(chǔ)特點和潛在需求規(guī)模���,有所側(cè)重地重點支持若干生物醫(yī)藥關(guān)鍵技術(shù)創(chuàng)新和產(chǎn)業(yè)化����,以便在“健康中國”建設(shè)進(jìn)程中進(jìn)一步提升我國生物醫(yī)藥產(chǎn)業(yè)國際競爭力,進(jìn)一步增進(jìn)我國人民健康水平和福祉����。
綜上,我們基于上一節(jié)梳理挖掘的全球主要國家重點資助的生物醫(yī)藥關(guān)鍵技術(shù)��,從未來生物醫(yī)藥產(chǎn)業(yè)的技術(shù)屬性和產(chǎn)業(yè)屬性兩個維度出發(fā)��,構(gòu)建技術(shù)性(包括對我國人民普遍生命健康安全的重要程度��、在我國的研發(fā)基礎(chǔ)����、我國通過自主研發(fā)或聯(lián)合開發(fā)實現(xiàn)該技術(shù)突破的難度)和產(chǎn)業(yè)化(包括對拉動經(jīng)濟(jì)增長的重要程度�、預(yù)期實現(xiàn)產(chǎn)業(yè)化或投入商業(yè)應(yīng)用所需的時間、產(chǎn)業(yè)化綜合成本)的二維指標(biāo)體系(見表2)����。
基于這一指標(biāo)體系,我們運(yùn)用德爾菲專家咨詢法面向來自西湖大學(xué)��、北京大學(xué)、中國生物醫(yī)學(xué)工程學(xué)會�、國家信息中心���、部分跨國生物醫(yī)藥企業(yè)和國內(nèi)生物醫(yī)藥創(chuàng)業(yè)企業(yè)等單位的專家開展問卷調(diào)查�,從而識別在我國具有較高技術(shù)突破可能性和較大產(chǎn)業(yè)化經(jīng)濟(jì)價值的關(guān)鍵技術(shù)���,為制定更有針對性的未來生物醫(yī)藥產(chǎn)業(yè)扶持政策提供科學(xué)客觀的依據(jù)。
此次生物醫(yī)藥未來重點方向和領(lǐng)域評價通過問卷星編輯問卷并在線上進(jìn)行發(fā)放,累計發(fā)放問卷50份��,實際返回有效問卷44份���,問卷回收率88%����。在專家機(jī)構(gòu)方面��,高校生物醫(yī)藥領(lǐng)域?qū)<艺?9.1%�,科研院所生物醫(yī)藥領(lǐng)域?qū)<艺?3.6%,企業(yè)生物醫(yī)藥領(lǐng)域?qū)<艺?0.5%��,政府部門生物醫(yī)藥領(lǐng)域?qū)<艺?.3%�,其他生物醫(yī)藥領(lǐng)域?qū)<艺?.6%。
表2未來生物醫(yī)藥關(guān)鍵領(lǐng)域技術(shù)評價指標(biāo)體系
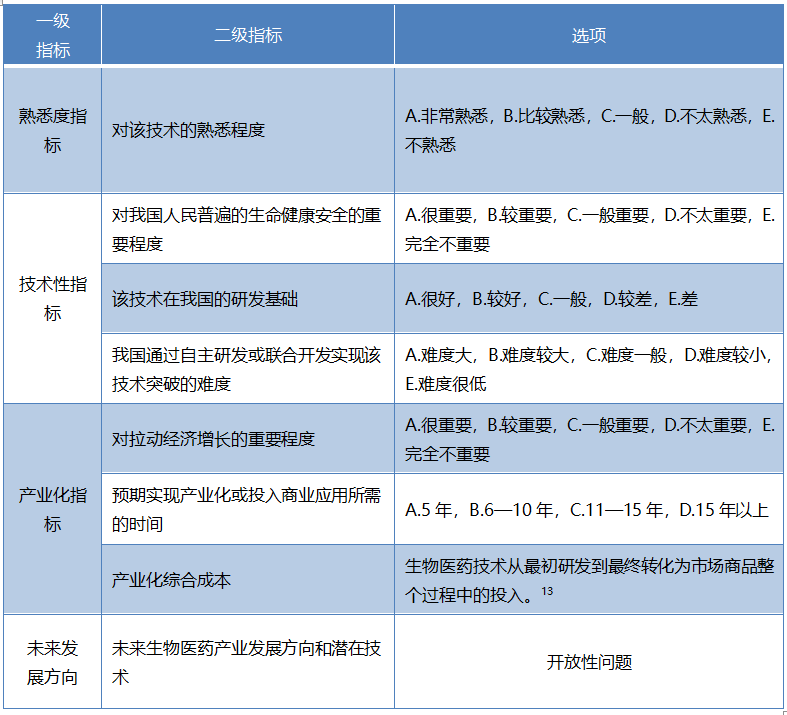
通過對問卷進(jìn)行賦值分析�,我們對技術(shù)池中30個關(guān)鍵技術(shù)從技術(shù)性得分(該技術(shù)的社會價值以及在我國實現(xiàn)突破的難易程度)和產(chǎn)業(yè)化得分(該技術(shù)的經(jīng)濟(jì)價值和在我國實現(xiàn)產(chǎn)業(yè)化的難易程度)兩個維度進(jìn)行刻畫賦值,給出最終的生物醫(yī)藥領(lǐng)域關(guān)鍵技術(shù)的在我國實現(xiàn)突破可能性大小和產(chǎn)業(yè)化難度高低的總和排序結(jié)果����。其中,技術(shù)性得分越高代表其社會價值越高且在我國實現(xiàn)突破的難度越?��?��;產(chǎn)業(yè)化得分越高代表其經(jīng)濟(jì)價值越高且實現(xiàn)產(chǎn)業(yè)化的綜合成本較低���。
表3 未來生物醫(yī)藥領(lǐng)域關(guān)鍵技術(shù)的技術(shù)性和產(chǎn)業(yè)化得分排名

圖4 30項關(guān)鍵技術(shù)綜合得分圖

從圖4可知���,在技術(shù)性方面�,高通量測序��、重組抗體�、抗體藥物偶聯(lián)物、誘導(dǎo)型人工多能干細(xì)胞��、人工智能+生物醫(yī)藥���、蛋白質(zhì)組學(xué)��、小分子抑制劑����、3D打印��、CRISPR-Cas、免疫檢查點抑制劑���、嵌合抗原受體�、基因編輯�����、mRNA疫苗等技術(shù)性綜合得分排名相對靠前���,反映了這些關(guān)鍵技術(shù)社會價值較高且在我國實現(xiàn)突破的難度較小��。在產(chǎn)業(yè)化方面��,人工智能+生物醫(yī)藥�����、免疫檢查點抑制劑��、小分子抑制劑�、藥物遞送����、3D打印�����、重組抗體����、抗體藥物偶聯(lián)物�����、mRNA疫苗�、CRISPR-Cas�����、嵌合抗原受體��、高通量測序�、靶向蛋白質(zhì)降解、蛋白質(zhì)組學(xué)等技術(shù)產(chǎn)業(yè)化綜合得分排名相對靠前��,反映了這些技術(shù)經(jīng)濟(jì)價值較高且實現(xiàn)產(chǎn)業(yè)化的綜合成本較低�。
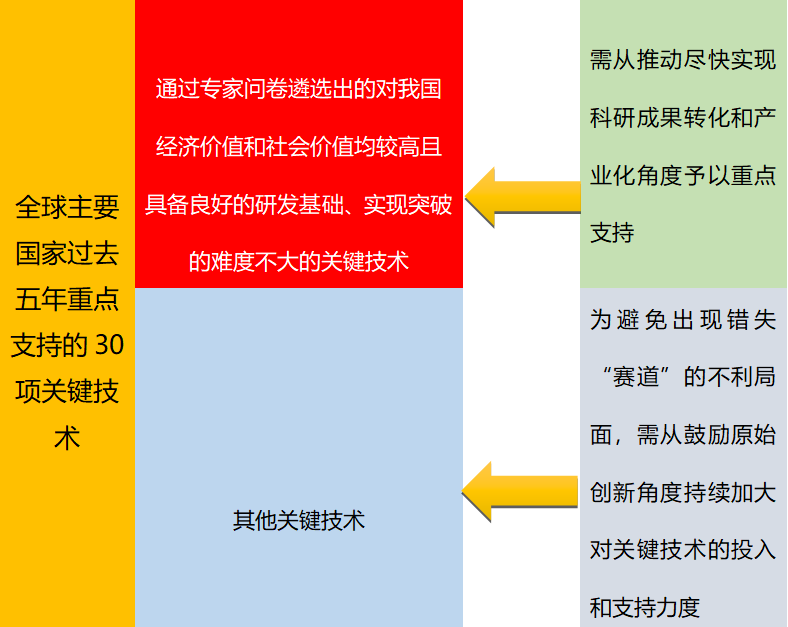
在圖4上可以發(fā)現(xiàn),未來生物醫(yī)藥產(chǎn)業(yè)關(guān)鍵技術(shù)的技術(shù)性綜合得分排名和產(chǎn)業(yè)化綜合得分排名具有一定的正相關(guān)性��,即技術(shù)性綜合得分排名靠前的關(guān)鍵技術(shù),其產(chǎn)業(yè)化綜合得分排名也相對靠前�。基于這一特征�,我們可以大致將圖5劃分為兩個部分,即總體處于右上角的技術(shù)���,包括人工智能+生物醫(yī)藥�����、重組抗體��、高通量測序�、抗體藥物偶聯(lián)物���、小分子抑制劑��、3D打印��、CRISPR-Cas���、免疫檢查點抑制劑、藥物遞送��、蛋白質(zhì)組學(xué)、mRNA疫苗���、嵌合抗原受體等���。這些關(guān)鍵技術(shù)的經(jīng)濟(jì)價值和社會價值均較高,產(chǎn)業(yè)化綜合成本較低����,預(yù)期實現(xiàn)時間也較短,同時這些技術(shù)具備良好的研發(fā)基礎(chǔ)���,實現(xiàn)突破的難度不大?�?梢哉J(rèn)為這些技術(shù)是我國未來生物醫(yī)藥產(chǎn)業(yè)中具有較好發(fā)展前景的領(lǐng)域����,需要從產(chǎn)業(yè)發(fā)展方面予以特別關(guān)注和有力支持。
除上述關(guān)鍵技術(shù)以外的其他技術(shù)�,如表觀遺傳療法、相分離��、細(xì)胞重編程���、基因替代療法�、空間轉(zhuǎn)錄組學(xué)、異種移植��、抗逆轉(zhuǎn)錄病毒療法���、蛋白質(zhì)設(shè)計�、代謝組學(xué)等總體處于圖4-4的左下區(qū)域�����。這些技術(shù)盡管得到全球主要國家的高度關(guān)注和大力支持����,但受其在我國經(jīng)濟(jì)價值和社會價值總體相對較低、預(yù)期實現(xiàn)時間較長���、技術(shù)研發(fā)基礎(chǔ)薄弱����、自主創(chuàng)新實現(xiàn)突破難度較大等因素影響����,可以認(rèn)為這些技術(shù)是我國未來生物醫(yī)藥產(chǎn)業(yè)中發(fā)展動能尚不足的領(lǐng)域�����。但必須看到�,盡管這些技術(shù)仍然是全球主要國家高度關(guān)注并大力支持的領(lǐng)域���,國內(nèi)生物醫(yī)藥研發(fā)機(jī)構(gòu)需要持續(xù)關(guān)注���、密切跟蹤這些關(guān)鍵技術(shù)發(fā)展情況,避免出現(xiàn)錯失“賽道”的不利局面(見表4)�。為此,需要在科研層面進(jìn)一步加大對這些關(guān)鍵技術(shù)投入和支持�。
表4未來生物醫(yī)藥領(lǐng)域關(guān)鍵技術(shù)政策支持方式模式
(來源:醫(yī)前沿)